科研进展
兰州化物所纳米马达靶向抗肿瘤药物研究获新进展
近年来,针对抗肿瘤药物存在的毒副作用大、药效不理想和递送靶向性弱等问题,纳米马达靶向抗肿瘤药物已成为药学和临床研究的热点之一,H₂S作为气体信号分子在炎症调控和肿瘤治疗中的作用备受关注。
中国科学院兰州化学物理研究所天然药物与化学测量研究中心海军人才团队利用荧光-质谱成像联用动态可视化技术,揭示非甾体抗炎药-萘普生(NSAIDs)与H₂S协同增效同时减少萘普生副作用的作用机制(Anal. Chem.,96(2024) 18474–18482)。在此基础上,进一步提出H₂S在调节炎症的同时,可能通过影响肿瘤微环境、增强免疫应答而实现肿瘤治疗的新策略。
基于此,研究人员开发了一种可编程近红外触发纳米马达(NOSH@PEG-HCuSNPs),实现“光热消融-气体增敏-免疫激活”三重协同抗肿瘤的精准治疗新方案。研究表明,在4T1乳腺癌细胞实验中,纳米马达结合近红外光照后,细胞凋亡率提高至79%,ATP水平下降60%,并显著激活TNF、FoxO、MAPK等凋亡信号通路。在小鼠荷瘤模型中,该纳米马达能完全清除原发肿瘤,并通过免疫记忆效应,显著抑制远端肿瘤生长(体积减少80%)。
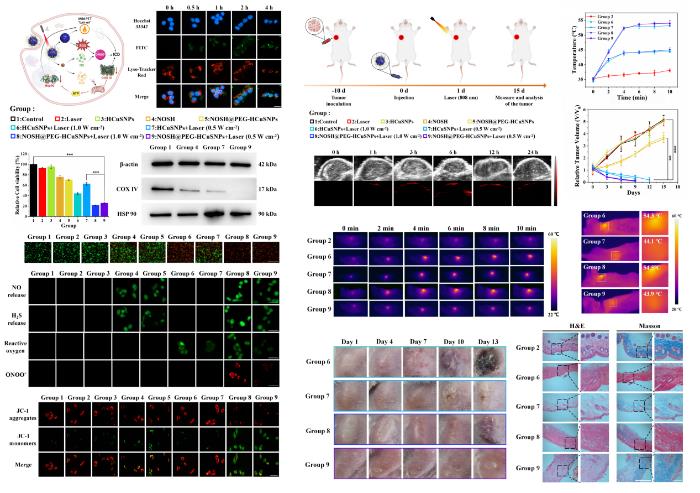
三重协同抗肿瘤活性评价
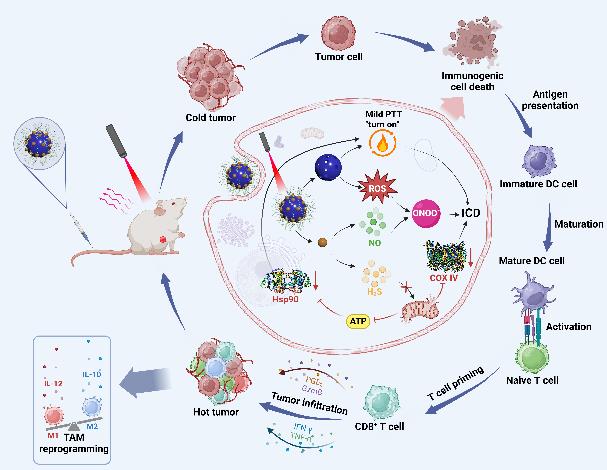
三重协同抗抗肿瘤作用机制
该研究利用双模态探针和荧光-质谱成像联用动态可视化技术,揭示了三重协同抗肿瘤的作用机制。结果表明,利用纳米马达,通过中空硫化铜纳米颗粒HCuSNPs负载气体信号分子供体NOSH,在808 nm激光照射下可控释放H₂S/NO,同时高效转换光能(光热转化效率达27.8%),确保局部温度维持在45℃以下,既能杀伤肿瘤细胞,又避免正常组织损伤。此外,该纳米马达不仅通过H₂S阻断线粒体能量代谢、NO-ROS反应生成ONOO⁻双路径诱导肿瘤凋亡,还可显著重塑肿瘤免疫微环境,促进M1型巨噬细胞极化(比例提升3倍)、CTLs浸润(增加5倍),全面提升免疫抗癌能力。
相关成果发表在Materials Today Bio(2025,31: 101540)上。兰州化物所张金龙助理研究员为论文第一作者,兰州化物所海军研究员、裴栋研究员,新疆大学李金耀教授、范仲雄副教授为论文共同通讯作者。
上述工作得到了国家自然科学青年基金、甘肃省自然科学基金等项目的支持。








